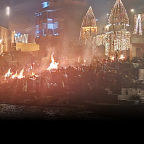![루마니아가 보낸 C-17 수송기가 27일 인천공항에서 한국산 방호복과 코로나19 진단키트를 싣고 있다. [뉴스1]](https://pds.joongang.co.kr/news/component/htmlphoto_mmdata/202003/31/261a79f5-1e99-4c94-84dc-7ff0a03c1000.jpg)
루마니아가 보낸 C-17 수송기가 27일 인천공항에서 한국산 방호복과 코로나19 진단키트를 싣고 있다. [뉴스1]
“한국의 진단 키트 제공 제안에 적절히 대응하지 못했다는 점을 후회한다. 치명적 실수였다. 사과하고 싶다.”(마그누스 헤우니케 덴마크 보건부 장관)
국내 4개 기업 47개국에 수출 중 #미 개발·양산 따로, 팬데믹 대처 못해 #유럽, 대기업 중심 의사결정 늦어 #국내 벤처, 중국 확산초기 개발 착수 #질본도 설연휴에 기업 소집해 독려
“코로나19 대처를 위해 (한국의) 의료장비를 지원해 줄 수 있나,”(도널드 트럼프 미국 대통령)
한국 바이오의 ‘신한류’다. 신종 코로나바이러스 감염증(코로나19)이 팬데믹(pandemic·전세계적 유행)으로 번지면서 세계 곳곳에서 한국 코로나19 진단키트를 보내달라는 ‘SOS’를 보내고 있다. 한국바이오협회에 따르면 씨젠과 코젠바이오텍·솔젠트·에스디바이오센서 등 식품의약품안전처의 긴급사용승인과 수출허가를 받은 국내 4개 기업이 세계 47개국에 진단키트를 수출하고 있다.
수출 으뜸은 4개 기업 중 유일한 상장사인 씨젠이다. 씨젠은 현재 1주일에 진단키트 100만 테스트(50만 명 분량)를 생산하고 있으며, 이 중 90% 이상을 해외에 공급하고 있다. 수출국은 유럽과 중동·동남아를 중심으로 총 45개국에 이른다. 최근 확진자가 급증하고 있는 미국의 경우, 지난 16일부터 식품의약국(FDA 승인을 받지도 않은 상태에서 추후 승인을 전제로 씨젠의 진단키트를 수입해 이미 사용하고 있는 것으로 밝혀졌다. 코로나19 발병 초기 한국 성지순례에 참여했던 관광객들을 억류했다 돌려보낸 이스라엘은 자국에서 쓰는 진단키트 전부를 씨젠에 의지하고 있다.
지난달 4일 국내에서 처음으로 긴급사용승인을 받은 코젠바이오텍도 현재 1주일에 25만 명을 진단할 수 있는 키트를 생산하고 있으며 이 중 70%를 수출하고 있다. 수출국이 다양한 씨젠과 달리 코젠은 사우디아라비아 등 중동 국가를 중심으로 30여 개국에 제품을 보내고 있다. 현재 국내에는 이들 기업 외에도 42개사 60여 개 제품이 질병관리본부의 긴급사용승인을 신청한 상태다.
왜 세계는 미국이나 유럽 등 기존 바이오과학 선진국이 아닌 한국, 그것도 중소기업의 진단키트에 목을 매고 있을까. 미국 대통령이 정상회담을 통해서까지 진단키트를 요청한 것은 전례가 없는 일이다.
우선 미국. 캘리포니아를 중심으로 첨단 바이오기업이 즐비한 미국에서 제대로 된 진단키트가 왜 없을까. 해답은 한국처럼 양산시설을 갖춘 기업이 진단시약과 키트를 개발하는 구조가 아니기 때문이다. 각 주의 질병통제센터(CDC)와 공공임상연구실이 자체적으로 진단시약을 개발하고 FDA의 승인을 얻어 감염병 진단에 대응하는 시스템이다. 그간은 팬데믹에 이를 정도로 감염 환자 폭증을 경험한 적이 없어 이들 기관의 생산만으로도 충분했다. 게다가 최근 개발한 코로나 진단키트에 오류가 생기면서 그나마도 공급이 더 늦어졌다. 결국 미국은 뒤늦게 다국적기업 로슈에 진단키트 공급을 요청했지만, 이마저도 부족한 상황이 됐다.
유럽은 어떨까. 이들 국가에도 바이오·제약 관련 글로벌기업이 있지만, 코로나19가 중국과 한국에서 번질 당시만 하더라고 ‘남의 나라 얘기’ 정도로 여겼다. 게다가 의사결정 과정이 늦은 대기업 중심이라 대응이 늦었다는 게 업계의 분석이다. 반면 한국은 중소벤처기업들이라 오너 중심의 빠른 결정을 내릴 수 있었다. 여기에 그간 쌓아 올린 노하우가 빛을 발했다. 국내 업체들은 기존 하루 이상 걸리던 진단을 대용량으로, 4~6시간 만에 해결했다. 진단 정확도도 98% 이상을 보였다. 체코·헝가리 등지에서 부정확한 진단으로 물의를 일으킨 중국 제품과는 비교가 안 된다.
체외진단기업협의회 운영위원을 맡은 오기환 한국바이오협회 전무는 “이번처럼 갑자기 코로나19 사태가 벌어질 때는 진단키트의 양산이 중요한데, 대량생산을 할 수 있는 것은 민간기업밖에 없다”며 “한국은 그간 사스와 메르스를 경험한 진단 관련 민간기업들이 노하우를 쌓아 빠르게 움직일 수 있었다”고 말했다.
오 전무는 질병관리본부의 발 빠른 대처도 높이 평가했다. 그는 “메르스를 경험한 질본이 기업에 긴급사용승인제를 통한 진단키트 개발을 요청한 것도 중요한 역할을 했다”고 덧붙였다. 긴급사용승인제도는 감염병 발생 때 절차를 건너뛰고 신규 진단 시약과 검사법을 즉시 사용할 수 있게 하는 것이다.
실제로 지난 1월 미국 국립생물공학정보센터(NCBI)에 코로나19의 유전자 염기서열이 공개된 지 14일만인 1월 26일, 설 연휴 중이었음에도 질병관리본부는 한국바이오협회에 진단키트 개발업체들을 모아 달라고 요청했다. 이튿날 곧바로 기업 대상 설명회가 열렸고, 28일 긴급사용승인 공고가 발표됐다. 2월 28일까지 한 달간 진단키트 개발 기업들의 신청을 받는다는 내용이었다. 이렇게 코젠바이오텍(2월4일)과 씨젠(2월13일)이 앞서 승인을 받았다. 긴급사용승인제가 없다면, 최소 1년 이상 걸리는 과정이었다.
국내 기업들은 질본보다 더 빨리 움직였다. 중국에서 코로나19가 빠르게 번져가는 가운데 염기서열이 공개되자 곧바로 진단키트 개발에 들어갔다.
천종윤 씨젠 대표는 “국제 사회에 코로나19 염기서열이 공개된 지 나흘 뒤인 1월 16일에 사내회의를 통해 코로나19 진단시약 개발을 제안하고, 21일 개발에 착수했다”며“당시엔 적자를 각오하는 심정으로 도전한 것”이라고 말했다.
최준호 과학·미래 전문기자 joonho@joongang.co.kr
![[오늘의 운세] 4월 24일](https://pds.joongang.co.kr/news/component/htmlphoto_mmdata/202404/24/9866f29c-fc4e-4fd9-ad4a-3d0a95d53514.jpg.thumb.jpg/_ir_432x244_/aa.jpg)